Марвелон таблетки №63
Форма выпуска: таблетки по 21 таблетке в блистере; по 1 блистеру в саше; по 1 или 3 саше в картонной упаковке
Группа: гормональные контрацептивы для системного применения
Подгруппа: эстрогены и гестагены в фиксированных комбинациях
Состав: 1 таблетка содержит 0,150 мг дезогестрела и 0,030 мг этинилэстрадиола (DESOGESTRELUM)
ИНСТРУКЦИЯ
для медицинского применения лекарственного средства
МАРВЕЛОН®
(MARVELON®)
Состав:
действующие вещества: desogestrel, ethinylestradiol;
1 таблетка содержит 0,150 мг дезогестрела и 0,030 мг этинилэстрадиола;
другие составляющие: крахмал картофельный; кремния диоксид коллоидный безводный; альфа-токоферол; кислота стеариновая; повидон; лактоза, моногидрат.
Лекарственная форма. Таблетки.
Основные физико-химические свойства: круглые, двояковыпуклые таблетки белого цвета, с одной стороны оттеснено слово ORGANON*, с другой - надпись TR/5.
Фармакотерапевтическая группа.Мочеполовая система и половые гормоны. Половые гормоны и модуляторы половой системы. Гормональные контрацептивы для системного использования. Эстрогены и гестагены в фиксированных комбинациях. Код ATX G03A A09.
Фармакологические свойства.
Фармакодинамика.
Марвелон - это комбинированное пероральное контрацептивное средство, содержащее 150 мкг дезогестрела и 30 мкг этинилэстрадиола.
Этинилэстрадиол - хорошо известный синтетический эстроген.
Дезогестрел - это синтетический прогестаген. После перорального применения оказывает мощное действие, направленное на ингибирование овуляции, проявляет мощную прогестагенную и антиэстрогенную активность, не проявляет эстрогенной активности, демонстрирует очень слабую андрогенную/анаболическую активность.
Фармакокинетика дезогестрела.
Всасывание.Дезогестрел, принимаемый перорально, быстро и полностью всасывается и превращается в этоногестрел. Пиковая концентрация в сыворотке крови составляет около 2 нг/мл приблизительно через 1,5 ч после применения разовой дозы. Биодоступность составляет 62 - 81%.
Деление. Этоногестрел связывается с сывороточным альбумином и глобулином, связывающим половые гормоны (ГСХ). Только 2 - 4% общей концентрации лекарственного средства в сыворотке крови присутствуют в виде свободного стероида, а 40 - 70% специфически связаны с ГЗСГ. Вызванное этинилэстрадиолом увеличение ГВСГ влияет на распределение между белками сыворотки крови, тем самым вызывает увеличение ГСПГ - связанной фракции и уменьшение связанной с альбумином. Ожидаемый объем распределения дезогестрела - 1,5 л/кг.
Метаболизм.Этоногестрел полностью метаболизируется известными способами метаболизма стероидов. Скорость выведения метаболитов из сыворотки крови составляет около 2 мл/мин/кг. Взаимодействия с принимаемым сопутствующим этинилэстрадиолом не выявлено.
Вывод. Уровни этоногестрела в сыворотке крови уменьшаются в два этапа. Конечный этап вывода характеризуется временем полувыведения примерно 30 часов. Дезогестрел и его метаболиты выводятся с мочой и желчью в соотношении примерно 6:4.
Состояние равновесия. Уровень ГОСГ, возрастающий втрое под действием этинилэстрадиола, влияет на фармакокинетику этоногестрела. После ежедневного применения уровень вещества в сыворотке крови возрастает примерно в 2-3 раза, достигая стабильной концентрации во второй половине цикла применения лекарственного средства.
Фармакокинетика этинилэстрадиола.
Всасывание. После перорального применения этинилэстрадиол быстро и полностью всасывается. Максимальная концентрация в сыворотке крови на уровне примерно 80 пг/мл достигается в течение 1-2 часов. Абсолютная биодоступность вследствие пресистемной конъюгации и первого этапа метаболизма составляет около 60%.
Деление. Этинилэстрадиол характеризуется сильным, но неспецифическим связыванием с сывороточным альбумином (приблизительно 98,5%) и приводит к повышению сывороточной концентрации ГВСГ. Определено, что ожидаемый объем распределения - 5 л/кг.
Метаболизм.Пресистемное конъюгирование этинилэстрадиола происходит как в слизистой тонкого кишечника, так и в печени. Этинилэстрадиол сначала метаболизируется путем ароматического гидроксилирования с образованием большого количества гидроксилированных и метилированных метаболитов, которые присутствуют как свободные метаболиты и как соединения с глюкуронидами и сульфатами. Скорость метаболического клиренса - примерно 5 мл/мин/кг.
Вывод. Уровень этинилэстрадиола в плазме крови уменьшается в два этапа, конечный этап выведения характеризуется временем полувыведения примерно 24 часа. В неизмененном виде этинилэстрадиол не выводится; выведение метаболитов этинилэстрадиола происходит вместе с мочой и желчью в соотношении 4:6. Период полувыведения метаболитов - примерно 1 сутки.
Состояние равновесия.Равновесные концентрации достигаются через 3-4 дня, когда уровень в сыворотке крови на 30-40% превышает концентрацию после однократной дозы.
Клинические свойства.
Показания.
Пероральная контрацепция.
При рассмотрении вопроса о назначении лекарственного средства Марвелон следует принимать во внимание индивидуальные риски у каждой отдельной женщины, особенно риск развития венозного тромбоэмболизма (ВТЭ), а также сравнить риск развития ВТЭ при применении лекарственного средства Марвелон и других комбинированных гормональных контрацептивов (см. разделы "Противопоказания" и "Особенности применения").
Противопоказания.
Комбинированные гормональные контрацептивы (КГК) нельзя применять при наличии каких-либо нижеперечисленных состояний. Если при использовании КГК впервые появляются какие-либо из перечисленных ниже состояний, применение средства следует немедленно прекратить.
Наличие или риск развития венозного тромбоэмболизма (ВТЭ).
· Венозный тромбоэмболизм - наличие ВТЭ ныне (проводится лечение антикоагулянтами) или в анамнезе (например тромбоз глубоких вен (ТГВ) или эмболия легочных сосудов (ЭЛС)).
· известные приобретенные или наследственные факторы риска развития венозного тромбоэмболизма, такие как резистентность к активированному протеину С (включая V фактор Лейдена), дефицит антитромбина III, дефицит протеина С, дефицит протеина S.
· обширное хирургическое вмешательство с длительной иммобилизацией (см. раздел «Особенности применения»).
· высокий риск развития венозного тромбоэмболизма вследствие наличия множественных факторов риска (см. раздел «Особенности применения»).
Наличие или риск развития артериального тромбоэмболизма (АТЕ)
- Артериальный тромбоэмболизм - наличие артериального тромбоэмболизма в настоящее время или в анамнезе (например инфаркт миокарда) или продромального состояния (например стенокардия).
- Цереброваскулярное заболевание - наличие инсульта, в анамнезе - инсульт или продромальное состояние (например транзиторное ишемическое нарушение мозгового кровообращения).
- Известна наследственная или приобретенная предрасположенность к развитию артериального тромбоэмболизма, например гипергомоцистеинемия и антитела к антифософолипидам (антитела к антикардиолипинам, волчаночный антикоагулянт).
- Мигрень в анамнезе с фокальными неврологическими симптомами.
- Высокий риск развития артериального тромбоэмболизма вследствие наличия множественных факторов риска (см. раздел «Особенности применения») или одного серьезного фактора риска:
- сахарный диабет с сосудистыми осложнениями;
- тяжелая форма артериальной гипертензии;
- тяжелая форма дислипопротеинемии.
Панкреатит или ранее перенесенный панкреатит, который ассоциируется с высокой гипертриглицеридемией.
Наличие в настоящее время или в анамнезе тяжелых заболеваний печени (пока показатели функции печени не вернутся в норму).
Наличие в настоящее время или в анамнезе опухолей печени (доброкачественных или злокачественных).
Установленные или подозреваемые эстрогензависимые опухоли (см. раздел «Особенности применения»).
Гиперплазия эндометрия.
Вагинальное кровотечение неустановленной этиологии.
Установленная или возможная беременность.
Повышенная чувствительность к любому активному или вспомогательному ингредиенту.
Марвелон противопоказано применять с комбинированной схемой лечения гепатита С, содержащей омбитасвир/паритапревир/ритонавир с дасабувиром или без него или препараты, включающие глекапревир/пибрентасвир (см. раздел «Особенности применения»).
Взаимодействие с другими лекарственными средствами и другими видами взаимодействий.
Предостережение. Необходимо внимательно прочитать инструкцию по медицинскому применению сопутствующего лекарственного средства для установления возможных взаимодействий.
Взаимодействие между пероральными контрацептивами и другими лекарственными средствами может привести к прорывному кровотечению и/или неэффективности перорального контрацептива. О нижеперечисленных взаимодействиях сообщается в литературных источниках.
Метаболизм в печени.Возможно взаимодействие с лекарственными или растительными средствами, индуцирующими микросомальные ферменты, в частности ферменты Р450 (CYP), что приводит к повышенному клиренсу половых гормонов и может снизить эффективность комбинированных пероральных контрацептивов, в том числе лекарственного средства Марвелон. К таким лекарственным средствам относятся фенитоин, фенобарбитал, примидон, босентан, карбамазепин, рифампицин и, возможно, окскарбазепин, топирамат, фельбамат, гризеофульвин, некоторые ингибиторы протеазы ВИЧ (например ритонавир) и ненуклеозидные ингибиторы содержат растительный компонент зверобой.
Индукция ферментов может наблюдаться спустя несколько дней лечения. Максимальная индукция ферментов обычно наблюдается в течение нескольких недель. После прекращения применения лекарственного средства индукция ферментов может продолжаться в течение примерно 28 дней.
При сопутствующем применении с гормональными контрацептивами многие ингибиторы протеазы ВИЧ (например нелфинавир) и ненуклеозидных ингибиторов обратной транскриптазы (например невирапин) и/или лекарственные средства против вируса гепатита С (ВГС) (например боцепревер, телопревер) могут увеличивать или уменьшать. в том числе этоногестрела, активного метаболита дезогестрела, или эстрогенов. Чистый эффект этих изменений в некоторых случаях может оказаться клинически значимым.
Женщинам, принимающим любое из этих лекарственных или растительных средств, индуцирующих ферменты печени, следует иметь в виду, что эффективность лекарственного средства Марвелона может быть снижена. При приеме средств, стимулирующих микросомальные ферменты, следует применять барьерный метод контрацепции в качестве дополнения к лекарственному средству Марвелон на протяжении всего срока применения лекарственного средства, стимулирующего микросомальные ферменты, и в течение 28 дней после прекращения применения такого лекарственного средства.
Если период приема сопутствующего лекарственного средства распространяется за пределы приема активных таблеток из КПК упаковки, следующую упаковку следует начинать без обычного перерыва в применении таблеток. При длительном лечении ферментостимулирующими средствами следует рассмотреть альтернативный метод контрацепции, на который не влияют лекарственные средства, стимулирующие микросомальные ферменты.
Одновременное применение с мощными (например кетоконазол, итраконазол, кларитромицин) или умеренными (например флуконазол, дилтиазем, эритромицин) ингибиторами CYP3A4 может привести к повышению сывороточных концентраций эстрогенов или прогестинов, в том числе этаногестрела, активного.
Пероральные контрацептивы могут оказывать влияние на метаболизм других лекарственных средств. Соответственно, в плазме крови и в тканях концентрации таких лекарственных средств могут повышаться (например, циклоспорина) или снижаться (например, ламотриджина).
В ходе клинических исследований комбинированной схемы лечения гепатита С, содержащей омбитасвир/паритапревир/ритонавир с дасабувиром или без него, повышение уровней АЛТ более чем в 5 раз выше верхнего предела нормы (ВМН) достоверно чаще встречалось у женщин, применявших средства, содержащие этинилэстрадиол (КГК). Также у женщин, применявших этинилэстрадиол (КГК), наблюдалось повышение уровня АЛТ при одновременном применении препаратов глекапревира/пибрентасвира. Применение Марвелона следует прекратить до начала комбинированного лечения гепатита С, содержащего омбитасвир/паритапревир/ритонавир с дасабувиром или без него или препараты глекапревира/пибрентасвира (см. разделы «Противопоказания» и «Особенности применения»). Возобновлять применение Марвелона следует примерно через 2 недели после завершения комбинированного лечения.
Лабораторные анализы Использование контрацептивных стероидов может повлиять на результаты определенных лабораторных тестов, включая биохимические показатели функций печени, почек, щитовидной железы, надпочечников, уровень белков (переносчиков) в сыворотке крови, например глобулина, связывающего кортикостероиды// показатели углеводного обмена, коагуляции и фибринолиза Изменения обычно остаются в пределах нормы.
Особенности применения.
При наличии любого из указанных ниже состояний/факторов риска назначения терапии лекарственным средством Марвелон следует обсудить с женщиной. При обострении, усилении или первом появлении любого из этих состояний женщина должна обратиться к врачу. Врач должен определить, следует ли прекратить применение КГК.
Нарушение кровообращения.
Риск развития венозного тромбоэмболизма (ВТЭ)
Применение любого КГК повышает риск развития венозного тромбоэмболизма (по сравнению с риском, когда КГК не используются). Лекарственные средства, содержащие левоногестрел, норгестимат или норетистерон, ассоциированы с минимальным риском развития ВТЭ. Другие лекарственные средства, такие как Марвелон, могут повышать риск в 2 раза. Решение о применении любого контрацептива, не являющегося лекарственным средством с минимальным риском развития ВТЭ, можно принимать только после обсуждения с женщиной рисков развития ВТЭ при применении лекарственного средства Марвелон®, влияния его индивидуальных факторов на этот риск, а также того, что риск развития ВТЭ является максимальным в течение первого года применения лекарственного средства. Также риск повышается при возобновлении применения КГК, если перерыв составлял 4 недели или больше.
Среди женщин, не применяющих КГК и не беременных, у двух из 10 000 будет развиваться ВТЭ в течение первого года. Однако у каждой отдельной женщины риск может быть гораздо выше в зависимости от основных факторов риска.
Установлено1, что из 10 000 женщин, применяющих КГК, содержащий дезогестрел, у 9 - 12 женщин через 1 год будет развиваться ВТЭ; для сравнения при применении КГК, содержащих левоногестрел, ВТЭ будет возникать у 62 женщин.
В обоих случаях количество случаев ВТЭ в год меньше, чем ожидаемое количество при беременности и в послеродовой период.
ВТЭ может быть летальным в 1 - 2% случаев.
1 Частота установлена по данным эпидемиологического исследования с использованием относительных рисков для различных лекарственных средств по сравнению с КГК, содержащими левоногестрел.
2 Средний диапазон от 5 до 7 на 10 000 женщин-лет установлен по относительному риску при применении КГК, содержащих левоногестрел, по сравнению с неприменением средства - от 2,3 до 3,6.
Количество случаев ВТЭ на 10000 женщин за 1 год
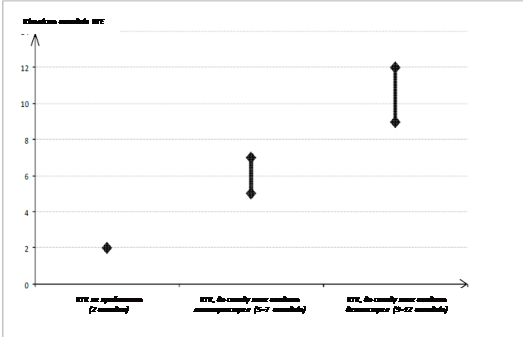 |
- Очень редко сообщалось о тромбозе, возникавшем в других кровеносных сосудах, например печеночных, мезентериальных, почечных, мозговых или ретинальных венах и артериях, у женщин, применявших КГК.
Факторы риска развития ВТЭ
- При применении КГК риск тромбоэмболических венозных осложнений может значительно повышаться у женщин с дополнительными факторами риска, особенно при наличии множественных рисков (см. таблицу 1).
- Лекарственное средство Марвелон противопоказано женщинам с множественными факторами риска, которые приводят к высокому риску развития венозного тромбоза (см. «Противопоказания»). Если у женщины более одного фактора риска, возможно, что мера повышения риска будет выше, чем сумма индивидуальных факторов. В этом случае следует проанализировать общий риск развития ВТЭ у женщины. Если соотношение преимуществ и рисков неблагоприятно, не следует назначать КГК (см. раздел «Противопоказания»).
Таблица 1
Факторы риска ВТЭ
| Фактор риска | Комментарий |
| Ожирение (индекс массы тела (ИМТ) более 30 кг/м2). | Риск значительно увеличивается при увеличении ИМТ. Особенно важно учитывать наличие других факторов риска. |
| Продолжительная иммобилизация, обширное хирургическое вмешательство, любое хирургическое вмешательство на ногах или органах таза, нейрохирургия, большая травма. Примечание. Временная иммобилизация, включая авиаперелеты продолжительностью более 4 часов, также может являться фактором риска развития ВТЭ, особенно у женщин с другими факторами риска. | Рекомендуется прекратить использование пластыря/таблеток/кольца (в случае элективной хирургии - как минимум за 4 недели до ее проведения) и не возобновлять раньше чем через 2 недели после полного восстановления подвижности. Во избежание беременности следует использовать другие средства контрацепции. Следует рассмотреть вопрос об антитромботической терапии, если применение лекарственного средства Марвелон не было прекращено заранее. |
| Положительный семейный анамнез (венозный тромбоэмболизм у брата/сестры или родителей, особенно в раннем возрасте, то есть до 50 лет). | Если подозревается наличие врожденной склонности, перед принятием решения о применении КГК женщину следует направить на консультацию к специалисту. |
| Другие медицинские состояния, сопровождающиеся ВТЭ. | Рак, системная красная волчанка, гемолитический уремический синдром, хроническое воспалительное заболевание кишечника (болезнь Крона или язвенный колит) и серповидноклеточная анемия. |
| Возраст | Особенно после 35 лет. |
- Нет единого мнения о возможной роли варикоза вен и поверхностного тромбофлебита в возникновении или прогрессировании венозного тромбоза.
- Следует учитывать повышенный риск тромбоэмболизма в период беременности, особенно в течение 6 недель после родов (см. раздел «Применение в период беременности или кормления грудью»).
Симптомы ВТЭ (тромбоз глубоких вен и эмболия легочных сосудов)
В случае возникновения симптомов женщина должна немедленно обратиться за медицинской помощью, сообщив врачу о том, что она принимает КГК.
Симптомы тромбоза глубоких вен (ТГВ) могут включать:
односторонний отек ноги и/или стопы или отек по ходу вены ноги;
- боль или болезненность в ноге, которая ощущается только при стоянии или ходьбе;
- более теплая на ощупь пораженная конечность; краснота или изменение цвета кожи ноги.
Симптомы эмболии легочных сосудов могут включать:
- внезапную одышку или быстрое дыхание;
- внезапный кашель, который может сопровождаться кровохарканью;
- острая боль в грудной клетке;
- сильное головокружение;
- быстрое или нерегулярное сердцебиение.
Некоторые из этих симптомов (например одышка, кашель) неспецифичны и могут быть ошибочно приняты за часто возникающие или менее тяжелые (например при инфекции респираторного тракта).
Другие признаки окклюзии сосудов могут включать внезапную боль, отечность и слегка синюшный оттенок кожи конечности.
Если происходит окклюзия сосудов глаза, симптомы могут варьировать от болезненной нечеткости зрения до потери зрения. Иногда потеря зрения может возникать практически немедленно.
Риск артериального тромбоэмболизма (АТЕ)
· эпидемиологические исследования установили связь между применением КГК и повышенным риском развития артериального тромбоэмболизма (инфаркт миокарда) или нарушений мозгового кровообращения (таких как транзиторное нарушение мозгового кровообращения, инсульт). Артериальные тромбоэмболические реакции могут быть летальными.
Факторы риска развития АТЕ
· риск развития артериальных тромбоэмболических осложнений или нарушение мозгового кровообращения при применении КГК повышается у женщин с факторами риска (см. таблицу 2). Лекарственное средство Марвелон противопоказано женщинам с одним серьезным или с множественными факторами риска развития АТЕ, которые приводят к высокому риску артериального тромбоза (см. «Противопоказания»). Если у женщины более одного фактора риска, возможно, мера повышения риска будет больше суммы индивидуальных факторов. В этом случае следует проанализировать общий риск для женщины. Если считается, что соотношение преимуществ и рисков неблагоприятно, КГК назначать не следует (см. раздел «Противопоказания»).
Таблица 2
Факторы риска развития АТЕ
| Фактор риска | Комментарий |
| Возраст | Особенно после 35 лет. |
| Курение | При применении КГК женщине рекомендуется прекратить курение. Женщинам старше 35 лет, которые продолжают курить, настоятельно рекомендуется применять другой способ контрацепции. |
| Артериальная гипертензия | |
| Ожирение (индекс массы тела более 30 кг/м2) | Риск значительно увеличивается при увеличении ИМТ. Особенно важно учитывать наличие других факторов риска. |
| Положительный семейный анамнез (артериальный тромбоэмболизм у брата/сестры или родителей, особенно в раннем возрасте, то есть до 50 лет) | Если подозревается наличие врожденной предрасположенности, перед принятием решения о применении КГК женщину следует направить на консультацию к специалисту. |
| Мигрень | Повышение частоты или тяжести мигрени при применении КГК (что может являться продромальным симптомом при нарушении мозгового кровообращения) может быть причиной немедленной отмены лекарственного средства. |
| Другие медицинские состояния, сопровождающиеся побочными реакциями со стороны сосудов | Сахарный диабет, гипергомоцистеинемия, заболевания клапанов сердца, фибрилляция предсердия, дислипопротеинемия и системная красная волчанка. |
Симптомы АТЕ
При возникновении симптомов женщина должна немедленно обратиться за медицинской помощью, сообщив врачу о том, что она принимает КГК.
Симптомы нарушения мозгового кровообращения могут включать:
- внезапное онемение или слабость в области лица, в руке или ноге, особенно с одной стороны тела;
- внезапное нарушение походки, головокружение, нарушение равновесия или координации;
- внезапная спутанность сознания, нарушение речи или понимания;
- внезапное нарушение зрения в одном глазу или у обоих;
- внезапная интенсивная или длительная головная боль, возникшая без определенной причины;
- потеря сознания или обморок с/без судорог.
Временные симптомы указывают на транзиторную ишемическую атаку (ТИА).
Симптомы инфаркта миокарда могут включать:
- боль, дискомфорт, чувство давления, тяжести, сжатия или переполненности в грудной клетке, руке или ниже грудины;
- дискомфорт с иррадиацией в спину, челюсть, горло, руку, желудок;
- ощущение переполненности желудка, диспепсия или запор;
- потливость, тошнота, рвота или головокружение;
- чрезвычайная слабость, тревожность или одышка;
- быстрое и нерегулярное сердцебиение.
Опухоли
Определенные исследования показали повышенный риск рака шейки матки у женщин, которые в течение длительного времени применяют КПК, однако по-прежнему существует неопределенность в степени обусловления заболевания сопутствующими эффектами, например различиями в сексуальном поведении или другими факторами, как инфицирование вирусом папилломы человека ( ВПЧ).
· Метаанализ 54 эпидемиологических исследований показал, что существует незначительное увеличение относительного риска (ВР = 1,24) выявления рака молочной железы у женщин, на данный момент применяющих комбинированные пероральные контрацептивы (КПК). Случаи рака молочной железы, диагностируемые у женщин, принимающих КПК на данный момент или применявших КПК в последние десять лет, более вероятнее локализуются в молочной железе, чем диагностированные случаи рака у женщин, никогда не принимавших КПК.
· Рак молочной железы редко возникает у женщин до 40 лет, независимо от того, применяют ли они КПК. Поскольку этот фоновый риск возрастает с возрастом, дополнительное количество случаев рака молочной железы у тех женщин, которые применяют КПК теперь или применяли их раньше, мало по сравнению с общим риском развития рака молочной железы (см. график).
· важнейшим фактором риска рака молочной железы у тех, кто применяет КПК, является возраст, в котором женщина прекращает принимать КПК; чем старше женщина при прекращении применения, тем выше вероятность диагностирования рака молочной железы. Продолжительность применения менее важна и повышенный риск постепенно исчезает в течение 10 лет после прекращения применения УПК настолько, что через 10 лет риск уже не превышает обычный.
· Возможное повышение риска рака молочной железы следует обсудить с женщиной и учесть преимущества применения КПК с учетом данных о том, что КПК обеспечивают значительную защиту от риска развития некоторых других видов рака (рак яичников и эндометрия), см. ниже приведенный график.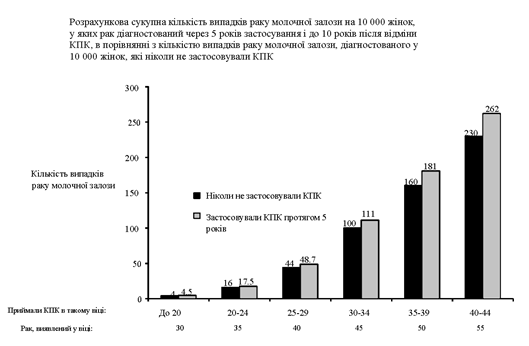
- В другом эпидемиологическом исследовании с участием 1,8 млн женщин из Дании, за которыми наблюдали в среднем 10,9 года, сообщалось, что ВР выявление рака молочной железы у применяющих КПК увеличивается при длительном их применении по сравнению с женщинами, которые никогда не применяли КПК (общий ВР = 1,19; показатель ВР находился в диапазоне от 1,17 при применении КПК от 1 до 5 лет и до 1,46 при применении КПК более 10 лет). Известная абсолютная разница в ВР (количество случаев возникновения рака молочной железы у женщин, никогда не применявших КПК, по сравнению с теми, кто применяет КПК сейчас или недавно закончили прием) было небольшим: 13 на 100 000 пациенто-лет.
· эпидемиологические исследования не предоставляют доказательств причинной обусловленности таких данных. Наблюдаемая модель повышенного риска может быть связана с более ранней диагностикой рака молочной железы у женщин, применявших КПК, биологическими эффектами КПК или комбинацией обоих факторов.
- У женщин, применявших КГК, в редких случаях сообщалось о доброкачественных и, гораздо реже, о злокачественных опухолях печени. В отдельных случаях такие опухоли приводили к опасным для жизни внутрибрюшным кровотечениям. Таким образом, опухоли печени следует учитывать при дифференциальной диагностике, если у женщин, применяющих КГК, возникают боли в верхней части живота, наблюдаются увеличение печени или признаки внутрибрюшного кровоизлияния.
Гепатит С
· В ходе клинических исследований комбинированной схемы лечения гепатита С, содержащей омбитасвир/паритапревир/ритонавир с дасабувиром или без него, повышение уровня АЛТ более чем в 5 раз выше верхнего предела нормы (ВМН) достоверно чаще встречалось у женщин, применявших лекарственные средства, содержащие этинилэстрадиол (КГК). Также у женщин, применявших этинилэстрадиол (КГК), наблюдалось повышение уровня АЛТ при одновременном применении препаратов глекапревира/пибрентасвира. Применение Марвелона следует прекратить до начала комбинированного лечения гепатита С, содержащего омбитасвир/паритапревир/ритонавир с дасабувиром или без него или глекапревир/пибрентасвир (см. разделы «Противопоказания» и «Взаимодействие с другими лекарственными средствами и другие виды взаимодействий»).
Прочие состояния.
· При применении КПК у женщин с гипертриглицеридемией или с ее наличием в семейном анамнезе возможен повышенный риск развития панкреатита.
· Экзогенные эстрогены могут вызвать или усилить симптомы наследственного и приобретенного ангионевротического отека.
· Хотя сообщалось о незначительном повышении артериального давления у многих женщин, принимающих КПК, клинически значимые повышения встречаются редко. Взаимосвязь между приемом КПК и клинической гипертензией не установлена. Однако если длительная клинически значимая артериальная гипертензия развивается на фоне применения КПК, врач должен запретить применение КПК и лечить артериальную гипертензию. Применение КПК можно восстановить при нормализации АД с помощью антигипертензивной терапии.
· сообщалось о возникновении или ухудшении таких состояний при беременности и при применении КПК: желтуха и/или зуд, связанные с холестазом; образование камней в желчном пузыре; порфирия; системная красная волчанка; гемолитико-уремический синдром; хорея Сиденгама; герпес беременных; потеря слуха, связанная с отосклерозом.
· Острые или хронические нарушения функции печени требуют немедленного прекращения использования КПК, пока печеночные пробы не вернутся к приемлемым показателям. Рецидивы желтухи и/или зуда, связанные с холестазом, которые возникали ранее во время беременности или половых стероидов, также требуют прекращения приема КПК.
· Хотя КПК могут влиять на периферическую резистентность к инсулину и нарушение толерантности к глюкозе, нет необходимости изменять схемы лечения больных сахарным диабетом, принимающих КПК. Однако, за женщинами, больными сахарным диабетом, должно быть тщательное наблюдение во время применения КПК.
· Хлоазма может периодически возникать, особенно у женщин с наличием в анамнезе хлоазмы беременных. Женщинам с предрасположенностью к хлоазме рекомендуется при применении данного лекарственного средства избегать пребывания на солнце или под действием ультрафиолетового излучения.
· Болезнь Крона и неспецифический язвенный колит связаны с приемом КПК.
· Лекарственное средство Марвелон содержит лактозу (<80 мг в 1 таблетке). При редкой наследственной непереносимости галактозы, лактазной недостаточности Лаппа или мальабсорбции глюкозы/галактозы не рекомендуется применять данное лекарственное средство.
Медицинское обследование
Перед началом или восстановлением применения лекарственного средства Марвелон врач должен внимательно ознакомиться с личным и семейным анамнезом женщины и исключить беременность. Учитывая противопоказания (см. раздел «Противопоказания») и оговорки (см. раздел «Особенности применения») относительно применения этого лекарственного средства, проводят полное медицинское освидетельствование и измеряют артериальное давление. Женщине следует предоставить информацию о венозном и артериальном тромбозах, включая данные о рисках при применении лекарственного средства Марвелон по сравнению с другими КГК, симптомов ВТЭ и АТЕ, известных факторов риска и действий при подозрении на тромбоз. Также женщине следует объяснить, что она должна тщательно перечитать инструкцию для медицинского применения лекарственного средства и придерживаться указанных в ней рекомендаций. Частоту и характер обследования определяет врач,
Женщину следует предупредить, что гормональные контрацептивы не защищают от ВИЧ-инфекции (СПИДа) и других заболеваний, передающихся половым путем. Если существует такой риск заражения (в том числе во время беременности или после родов), рекомендуется адекватное использование презерватива с другими методами контрацепции.
Уменьшение эффективности.
Эффективность применения лекарственного средства Марвелон может снижаться, например в случае пропуска применения таблеток, возникновения желудочно-кишечных расстройств (см. раздел «Способ применения и дозы») или при одновременном применении некоторых лекарственных средств, снижающих концентрацию в плазме крови этоногестрела, активного метаболита дезогестрела (см. раздел «Взаимодействие с другими лекарственными средствами и другие виды взаимодействий»).
Ухудшение контроля менструального цикла.
При применении КГК возможны нерегулярные (незначительные или обильные) кровотечения, особенно в первые месяцы применения. Поэтому оценка любых нерегулярных кровотечений может быть корректна только после адаптационного периода, который составляет примерно три цикла.
Если нерегулярные кровотечения сохраняются или возникают после предварительных регулярных циклов, следует рассмотреть негормональные причины и назначить адекватные диагностические мероприятия, включая кюретаж, для исключения беременности или злокачественной опухоли.
У некоторых женщин при интервале без таблеток кровотечение отмены может не наблюдаться. Если КГК применяли в соответствии с рекомендациями, приведенными в разделе «Способ применения и дозы», то возможность беременности невелика. Однако если были нарушения этих рекомендаций до первого отсутствия кровотечения отмены в период без таблеток или если кровотечения отмены отсутствуют дважды подряд, прежде чем продолжить принимать КГК, следует исключить возможную беременность.
Применение в период беременности или кормления грудью.
Беременность
Беременность является противопоказанием к применению лекарственного средства Марвелон®. Если женщина забеременела во время применения лекарственного средства Марвелон, дальнейшее применение следует прекратить. Однако расширенные эпидемиологические исследования не выявили ни повышения риска патологий у детей, матери которых принимали КПК до беременности, ни тератогенных эффектов КПК, которые непреднамеренно применяли в начале беременности.
Следует помнить о повышенном риске ВТЭ в послеродовой период при возобновлении применения лекарственного средства Марвелон (см. раздел «Способ применения и дозы» и «Особенности применения»).
Кормление грудью
КПК могут влиять на кормление грудью, поскольку они могут уменьшить количество и изменить состав грудного молока. Таким образом, применение КПК обычно не рекомендуется до полного окончания периода кормления грудью. С грудным молоком могут выделяться малые количества контрацептивных стероидов и/или их метаболитов, но нет никаких доказательств, что это оказывает негативное влияние на здоровье младенца.
Способность влиять на скорость реакции при управлении автотранспортом или другими механизмами.
Лекарственное средство не влияет на быстроту реакции при управлении автотранспортом или другими механизмами.
Способ применения и дозы.
Таблетки следует принимать в указанном на упаковке порядке, ежедневно примерно в одно и то же время, запивая при необходимости небольшим количеством жидкости. В течение 21 дня принимают по 1 таблетке. Таблетки из каждой последующей упаковки принимают после 7 дней без таблеток, в течение которого обычно происходит кровотечение отмены. Как правило, она начинается на 2 - 3-й день после применения последней таблетки и может продолжаться до начала применения таблеток из последующей упаковки.
Гормональные контрацептивы в предыдущий период (последний месяц) не применялись.
Применение таблеток начинают в первый день природного цикла женщины (т.е. в первый день менструального кровотечения). Можно начать применение со 2-5-го дня, однако в таком случае в течение первых 7 дней первого цикла применения таблеток рекомендуется дополнительно использовать барьерный метод контрацепции.
Переход из другого комбинированного гормонального контрацептива (комбинированного перорального контрацептива (КПК), вагинального кольца или трансдермального пластыря).
Желательно, чтобы женщина начала применение лекарственного средства Марвелон на следующий день после последнего применения активной таблетки (последней таблетки, содержащей активные субстанции) предыдущего КПК, но не позднее следующего дня после перерыва в применении таблеток или после применения неактивной таблетки предыдущего КПК. В случае использования вагинального кольца или трансдермального пластыря женщина должна начинать применение лекарственного средства Марвелон желательно в день удаления, но не позднее дня последующего применения.
Если предыдущий метод контрацепции использовался правильно и систематически и женщина уверена в том, что она не беременна, она также может перейти из другого комбинированного гормонального контрацептива в любой день цикла.
Период, свободный от применения гормонального контрацептива, не должен быть длиннее рекомендованного.
Переход из лекарственных средств, в которых содержится только прогестаген (мини-пили, инъекция или имплантат), или внутриматочной системы (ВМС), высвобождающей прогестаген.
Женщина может начинать применение лекарственного средства Марвелон в любой день после прекращения применения мини-пили (в случае имплантата или ВМС - в день его/ее удаления, в случае инъекции - в день следующей инъекции). Во всех случаях женщина должна использовать дополнительно барьерный метод контрацепции в течение первых 7 дней применения таблеток.
После аборта в первом триместре.
Женщина может начинать применение лекарственного средства сразу после аборта. В таком случае нет необходимости использовать дополнительные средства контрацепции.
После родов или аборта во втором триместре.
Применение лекарственного средства во время кормления грудью (см. раздел Применение в период беременности или кормления грудью).
Женщинам рекомендуется начинать применение с 21-го или 28-го дня после родов или аборта во втором триместре. Если применять лекарственное средство позже, рекомендуется дополнительно использовать барьерный метод в течение первых 7 дней применения таблеток. В любом случае, если в этот период уже были половые контакты, то перед началом применения КПК следует исключить беременность или подождать до первой менструации.
Как следует поступать в случае пропуска приема таблеток
Если женщина опоздала с применением следующей таблетки менее чем на 12 часов , противозачаточное действие лекарственного средства не уменьшается. Женщина должна принять таблетку, как только упомянет о ней, и дальше продолжать применение в обычное время.
Если женщина опоздала с применением следующей таблетки более чем на 12 часов , контрацептивная защита может уменьшаться. В этом случае действуют два основных правила:
1. Не прекращать применение таблеток более 7 дней.
2. После начала применения таблеток адекватное торможение оси гипоталамус - гипофиз - яичники достигается за 7 дней непрерывного применения.
Согласно этому в повседневной жизни следует руководствоваться следующими советами:
· Неделя 1.
Женщина должна принять последнюю пропущенную таблетку сразу же, как только упомянет о пропуске, даже если придется принять две таблетки одновременно. Далее она продолжает принимать таблетки в обычное время. Кроме того, в течение следующих 7 дней следует использовать барьерный метод контрацепции, например, презерватив. Если за предыдущие 7 дней были половые контакты, следует учитывать возможность возникновения беременности. Чем больше таблеток пропущено и чем ближе этот пропуск к обычному периоду без таблеток, тем больше риск беременности.
· неделя 2.
Женщина должна принять последнюю пропущенную таблетку сразу же, как только вспомнит пропуск, даже если придется принять две таблетки одновременно. Далее она продолжает принимать таблетки в обычное время. Если до пропущенной таблетки женщина в течение 7 дней правильно принимала предварительные таблетки, то дополнительные средства контрацепции не требуются. Однако в противном случае или если пропущено более одной таблетки, в течение следующих 7 дней следует использовать дополнительные методы контрацепции.
· неделя 3.
Риск понижения надежности возрастает с приближением перерыва в применении таблеток. Однако при соблюдении определенной схемы применения таблеток можно избежать снижения контрацептивной защиты. Если придерживаться одного из нижеприведенных вариантов, то не возникнет необходимости использовать дополнительные контрацептивные средства при условии, если женщина принимала таблетки правильно в течение 7 дней до пропуска. Если же это не так, то женщина должна соблюдать первый из следующих вариантов и использовать дополнительные меры предосторожности в течение следующих 7 дней.
1. Женщина должна принять последнюю пропущенную таблетку сразу же, как только вспомнит пропуск, даже если придется принять две таблетки одновременно. Далее она продолжает принимать лекарственное средство в обычное время. Таблетки из следующей упаковки следует начать принимать сразу же после окончания таблеток из предварительной упаковки, то есть не должно быть перерыва в применении лекарственного средства. Маловероятно, что у женщины начнется кровотечение отмены до окончания применения таблеток из второй упаковки, хотя в процессе приема возможно кровомазание или внезапное кровотечение.
2. Женщина также может прекратить применение таблеток из используемой упаковки. В этом случае перерыв должен составлять 7 дней, включая дни пропуска таблеток; Применение таблеток следует начать со следующей упаковки.
Если женщина пропустила очередной прием таблеток и в течение первого планового периода без таблеток отмены кровотечения не было, возможно, она забеременела.
Рекомендации при желудочно-кишечных расстройствах.
В случае тяжелого желудочно-кишечного нарушения всасывание лекарственного средства может быть неполным, поэтому необходимо принимать дополнительные меры контрацепции. Если рвота случилась в течение 3-4 часов после применения таблетки, следует соблюдать рекомендации по пропущенным таблеткам (см. «Как следует поступать в случае пропуска приема таблеток»). Если женщина не хочет изменять свою привычную схему применения таблеток, она должна принять дополнительную таблетку из другой упаковки.
Как изменить или задержать начало менструации
Чтобы задержать начало менструации, женщине просто следует продолжать принимать таблетки из последующей упаковки и не делать перерывы. При желании возможна любая задержка в пределах количества таблеток второй упаковки вплоть до их окончания. При задержке у женщины может наблюдаться внезапное кратковременное кровотечение или кровомазание. После планового 7-дневного периода без таблеток возобновляется регулярный прием таблеток.
Чтобы переместить начало менструации на другой день недели от обычной схемы, женщине можно порекомендовать сократить ближайший период без таблеток на нужное количество дней. Чем меньше этот период, тем больше вероятность отсутствия кровотечения отмены и возникновения кровомазания и кратковременных кровотечений при применении следующей упаковки (как и при задержке месячных).
Дети
Нет клинических данных по эффективности и безопасности применения лекарственного средства детям (до 18 лет).
Передозировка.
О серьезных и опасных осложнениях при передозировке не сообщалось. При передозировке могут возникать следующие симптомы: тошнота, рвота, у девушек - незначительные кровянистые выделения из влагалища. Антидотов не существует, лечение передозировки должно быть симптоматическим.
Побочные реакции.
Описание отдельных побочных реакций
При применении КГК (комбинированных гормональных контрацептивов) наблюдался повышенный риск артериального и венозного тромбоэмболизма, включая инфаркт миокарда, паралич, транзиторное ишемическое нарушение мозгового кровообращения, тромбоз глубоких вен; Более подробную информацию см. в разделе «Особенности применения».
В начале применения КПК наблюдались изменения в характере вагинального кровотечения, особенно в первые месяцы приема, также фиксировались изменения частоты кровотечения (отсутствие, менее часто, более часто или длительно), интенсивность (уменьшение или увеличение) или изменение общей продолжительности вагинального кровотечения.
Возможные относительные побочные реакции1, о которых сообщалось при применении лекарственного средства Марвелон или КПК (комбинированные пероральные контрацептивы), отмечены в таблице 3. Все побочные реакции представлены по системам органов и частоте: часто (≥ 1/100), нечасто (≥ 1/ 1000, <1/100), редко (<1/1000), неизвестно (нельзя оценить по имеющимся данным).
Таблица 3
| Система органов | Часто | Нечасто | Редко | Неизвестно |
| Со стороны иммунной системы | Повышенная чувствительность | Обострение симптомов наследственного и приобретенного ангионевротического отека | ||
| Со стороны метаболизма и питания | Задержка жидкости | |||
| Психические расстройства | Депрессивное настроение, смена настроения | Снижение либидо | Повышение либидо | |
| Со стороны нервной системы | Головная боль | Мигрень | ||
| Со стороны органов зрения | Непереносимость контактных линз | |||
| Со стороны сосудов | Венозный тромбоэмболизм2, артериальный тромбоэмболизм2 | |||
| Со стороны пищеварительного тракта | Тошнота, боль в животе | Диарея, рвота | ||
| Со стороны кожи и подкожных тканей. | Сыпь, крапивница | Узловая эритема, мультиформная эритема | ||
| Со стороны репродуктивной системы и молочных желез | Боль в молочных железах, болезненность молочных желез | Гипертрофия молочных желез | Выделение из влагалища, выделение из молочных желез | |
| исследование | Увеличение массы тела | Уменьшение массы тела |
1 Наиболее приемлемый термин MedDRA для описания определенной нежелательной реакции. Синонимы или подобные состояния не перечислены, но также должны приниматься во внимание.
2 Частота наблюдений в когортных исследованиях от ≥ 1/10000 до 1/1000 женщин-лет
У женщин, принимавших комбинированные гормональные контрацептивы, были зафиксированы следующие побочные реакции: ангионевротический отек и/или обострение наследственного ангионевротического отека, акне, алопеция, кисты яичников, нарушение менструации, дисменорея, внематочная беременность, зуд, сон, усталость гинекомастия, предменструальный синдром, гирсутизм, изменение липидов в плазме крови, изменение аппетита. Более подробную информацию о побочных реакциях, о которых сообщалось при применении КПК (тромбоэмболические заболевания вен, тромбоэмболические заболевания артерий, артериальная гипертензия, гормонозависимые опухоли (например опухоли печени, рак молочных желез), хлоазма приведены в разделе «Особенности применения».
Данные о влиянии КПК на лабораторные анализы см. в разделе «Взаимодействие с другими лекарственными средствами и другие виды взаимодействий».
Срок годности. 3 года.
Условия хранения.
Хранить в оригинальной упаковке при температуре не выше 30 С в недоступном для детей месте.
Упаковка.
По 21 таблетке в блистере, по 1 блистеру в саше, по 3 саше в картонной коробке.
Категория отпуска. По рецепту.
Производитель.
Н.В. Органон.
Местонахождение производителя и его адрес места осуществления деятельности.
Юридический адрес: 5349 АВ Осс, Клоостерштраат 6, Нидерланды.
Адрес места осуществления деятельности: Моленштраат 110, 5342 СС Осс, Нидерланды.
Внимание!
Внимание! Цена, наличие товаров, условия доставки подтверждаются контакт-центром. Если вы заметили неточность, сообщите нам anri.content(sbk)ukr.net. Фотографии некоторых товаров могут отличаться.



